Zvanično: Njemačka odobrila vakcinu AstraZenece za starije od 65 godina
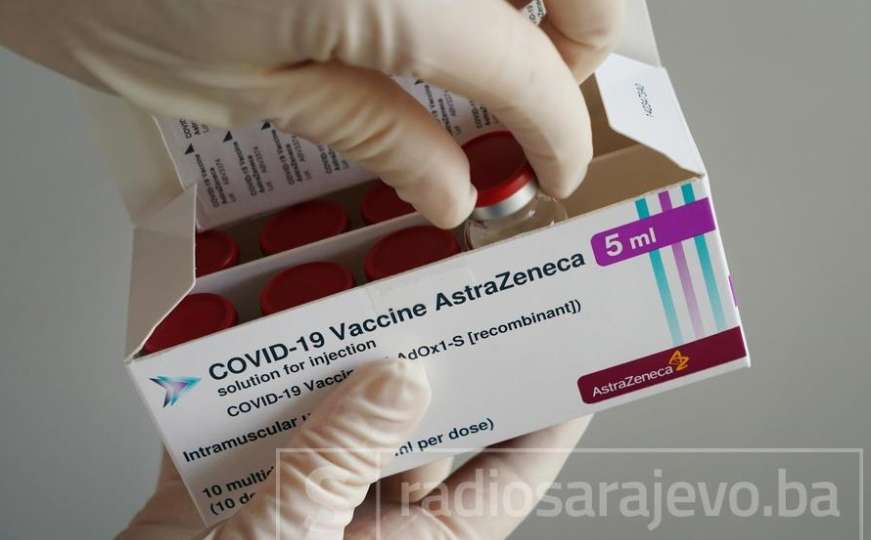
Njemačke zdravstvene vlasti odobrile su upotrebu cjepiva AstraZenece za starije od 65 godina, objavilo je ministarstvo zdravstva, što je korak koji će zasigurno pomoći da se ubrza spori ritam cijepljenja u zemlji.
Ministarstvo je također objavilo da je stalno državno tijelo zaduženo za cijepljenje preporučilo da se produlji razdoblje između prve i druge doze AstraZenecinog cjepiva, ali na maksimalno 12 sedmica, oslanjajući se na studije koje pokazuju da dulji razmak poboljšava njegovu učinkovitost.
"To su dobre vijesti za starije ljude koji čekaju na cjepivo. Sada će moći brže biti cijepljeni", istaknulo je ministarstvo koje je najavilo da će "ubrzo objaviti regulativu koja će omogućiti primjenu obiju preporuka".
Prvo su ga odbili koristiti za starije
Njemačka je prvobitno odbila korištenje cjepiva AstraZenece za starije od 65 godina, navodeći da nema dovoljno dokaza iz kliničkih testiranja o njegovoj učinkovitosti za stariju dobnu skupinu.
No sve veći broj podataka ukazao je na učinkovitost ovog cjepiva i na stariju populaciju u Britaniji, što je nagnalo Berlin na promjenu stajališta. Slično je postupila i Francuska.
Njemačka odluka saglasna je s preporukama zdravstvenog regulatora Europske unije koji savjetuje da se druga doza tog cjepiva uzme u razmaku od četiri do 12 sedmica od prve.
U priopćenju se ne spominje drugo cjepivo koje je odobreno u Njemačkoj, ono Pfizera i njemačkog BioNTecha.
Ministar Jens Spahn preporučio je da se to cjepivo primi s razmakom od šest tjedana iz praktičnih razloga slabe opskrbe cjepivom.
Regulator Europske unije zasad ostaje pri preporuci o razmaku od tri sedmice za to cjepivo, piše Hina.
Njemački političari našli su se na udaru sve žešćih kritika zbog sporog ritma cijepljenja u Njemačkoj, koji je daleko zaostao u odnosu na vodeće zemlje u cijepljenju Britaniju, Izrael i SAD.

Radiosarajevo.ba pratite putem aplikacije za Android | iOS i društvenih mreža Twitter | Facebook | Instagram, kao i putem našeg Viber Chata.









